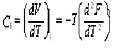Термодинамика
| Термодинамика |
|---|

|
| Бул макала бираталышттуу сериянын бөлүгү болуп саналат. |
| Термодинамиканын башталышы |
| Абалдардын теңделиши |
| Термодинамикалык чоңдуктар |
| Термодинамикалык потенциалдар |
| Термодинамикалык циклдер |
| Фазалык өтүүлөр |
| оңдоо |
| Кошумча к; «Физикалык портал» |
Термодинамика (грек. θέρμη — «сийдик», δύναμις — «бок») – термодинамикалык теңсалмактуулук абалдагы макросистемалардын эң жалпы касиеттери жана бул абалдардын биринен бирине өтүү процесстери жөнүндөгү илим.
Бул теория материяда өтүп жаткан бардык жылуулук (температуралык) өзгөрүүлөр менен улантылган, жалпыга белгилүү тажрыйбалык далилдерге негизделген ой жүгүртүүнүн жолу болуп саналат. Термодинамика теория катарында жылуулук машиналарын, б. а. жылуулуктун эсебинен жумуш аткарган машиналарды куруу тажрыйбаларын жалпылоонун негизинде келип чыккан. Термодинамика теориясы идеалдык газ түшүнүгүнө негизделип түзүлгөн. Заттардын реалдык абалдарын (катуу, суюк, газ) идеалдык газдардын (электрондук, фотондук, фонондук ж. б.) катарына ажыратууга болот. Мис., металлдардагы эркин электрондор тобу идеалдык газ катары каралышы мүмкүн. Термодинамиканын жардамы менен жаратылыштын ар кандай кубулуштарын (оптикалык, электрдик, магниттик, химиялык, механикалык ж. б.) изилдөөгө болот. Макросистемалардын физикалык касиеттерин өздөштүрүш үчүн бирин бири толуктаган Термодинамикалык жана статистикалык ыкмалар колдонулат. Заттын ички түзүлүшүнө көңүл бурбай туруп эле, анын макроскопиялык касиеттерин (көлөм, басым, температура, курам ж. б.) өздөштүрүүчү ыкма Термодинамикалык ыкма деп аталат. Бул ыкмадагы негизги физикалык чоңдук – энергия. Зат касиеттерин өздөштүрүүдө аны түзгөн бөлүкчөлөрдүн касиеттерине жана өз ара аракеттешүүлөрүнө таянган ыкма статистикалык ыкма деп аталат. Бул ыкма статистикалык физикада (термодинамикада) кеңири колдонулат. Башка бардык теориялар сыяктуу эле Термодинамика дагы өзүнө тиешелүү түшүнүктөргө таянат. Термодинамикалык системанын абалын мүнөздөөчү физикалык чоңдуктар Термодинамикалык өлчөмөлөр (параметрлер) деп аталат. Өлчөмөлөр ички жана тышкы болуп бөлүнөт. Ички жана тышкы өлчөмөлөрдүн ортосундагы байланышты аныктоо – Термодинамиканы чечүүчү маселелердин бири. Термодинамикалык системанын бир тектүү түзүүчүсү ф а з а деп аталат. Ушуга байланыштуу Термодинамикалык система бир фазалуу, эки фазалуу, көп фазалуу ж. б. болуп бөлүнөт. Реалдык Термодинамикалык системалар адатта көп фазалуу болот. Бир фазалуу система аркылуу көп фазалуу Термодинамикалык системаны өздөштүрүүгө (эсептөөгө) болот. Термодинамикалык системанын бир абалдан экинчисине которулушу Термодинамикалык жүрүш (процесс) деп аталат. Жүрүштөр теңсалмактуу жана теңсал-мактуу эмес, кайталануучу жана кайталанбоочу болуп бөлүнөт. Системанын абалын мүнөздөөчү өлчөмөлөрү өзгөрүүсүз улантылган жүрүш теңсал-мактуу жүрүш деп аталат. Жүрүш учурунда Термодинамикалык системанын өлчөмөлөрү өзгөрүп турса, анда ал теңсалмактуу эмес жүрүш болуп саналат.
Термодинамикада ар кандай жүрүштөр жогоруда келтирилген түшүнүктөр аркылуу жазылган Термодинамиканын негизги үч законунун жардамы менен изилденет. Термодинамиканын 1-башталышы энергиянын сакталуу жана айлануу закону болуп саналат: Q=dИ+А, мында dИ системанын ички энергиясынын өзгөрүшү, Qсистемага берилген жылуулук саны, Асистеманын тышкы күчкө каршы аткарган жумушу. Термодинамиканын 1-башталышы системадагы энергиянын сакталышын гана көрсөтөт. Ал эми Термодинамиканын 2-башталышы Термодинамикалык жүрүштүн багытын көрсөтөт: ар кандай физикалык жүрүштөр энергиянын бардык түрлөрү өзүнөн өзү жылуулук энергиясына айлангандай болуп өтөт. Демек макродүйнөдө дайыма температуралардын теңделиши болуп турат, б. а. ПАКи нөлгө умтулат. Натыйжада, системанын энтропиясы S өсө берет. Ошентип, dS QТ, мында dS энтропиянын өзгөрүшү, Т системанын температурасы. Бул 2 законду бириктирүүдөн Термодинамиканын негизги закону алынат: . (1). Мында барабардык кайталануучу жүрүшкө, барабарсыздык кайталанбоочу жүрүшкө туура келет. (1) туюнтма бойунча системадагы ар кандай жүрүш учурунда энтропиянын өзгөрүү чоңдугу эсептелет. (1) ден Т=const болгондо A=–d(U–ТS) келип чыгат, мында U – бул ТS системанын эркин энергиясы, б. а. системанын ички энергиясынын жумуш аткарган бөлүгү, ТS – байланыш энергиясы, б. а. системанын ички энергиясынын айлана-чөйрөгө тараган бөлүгү. Термодинамикалык системанын эркин энергиясынын өзгөрүшү Термодинамиканын 2-башталышы жана циклдик ыкманын жардамы менен чыгарылган Гиббс–Гельмгольц теңдемеси менен эсептелет. Термодинамикалык системадагы фазалык өтүш мезгилинде температура менен басымдын өзгөрүүлөрүн байланыштырган Клапейрон–Клаузиус теңдемеси да Термодинамиканын 2-башталышы жана циклдик ыкма менен алынат.
Термодинамикалык системанын касиеттерин өзү же туундусу аркылуу ачык туюндура алуучу функциялар Термодинамикалык потенциалдар делет. Кабыл алынган көзкаранды эмес чоңдуктарына жараша ар кандай Термодинамикалык потенциалдар колдонулат. Эгерде Термодинамикалык системанын курамы жана бөлүкчө саны өзгөрбөсө, анда көзкаранды эмес өзгөрмөлүү чоңдуктардын ар бир түгөйү үчүн төмөнкүдөй Термодинамикалык потенциалдар туура келет: ички энергия U=U(S,V); эркин энергия F=F(T,V); Гиббс Термодинамикалык потенциалы G=G(T, P); энтропия H=H(S, P). Термодинамикалык потенциалдарга көзкаранды эмес чоңдуктары бойунча алынган 1-же 2-туунду аркылуу системанын Термодинамикалык өлчөмөлөрүн эсептөөгө болот. Мис., системанын басымын (Р) табыш үчүн эркин энергиядан (F) турактуу температура учурунда көлөм бойунча 1-туунду алуу жетиштүү:
о. эле жол менен жылуулук сыйымдуулук табылат:
Бул Термодинамикалык потенциалдар ыкмасы илимдин бардык тармагында кеңири колдонулат. Термодинамиканын 3-башталышы 1-жана 2-башталышына салыштырмалуу толук иштелип чыга элек. Ошентсе да төмөнкү температурадагы тажрыйбалардын жыйынтыктарын жалпылоо жолу менен Термодинамиканын 3-башталышы (Нернст теоремасы) аныкталды: абсолюттук нөл температурасында ар кандай бирдей температуралык жүрүштөр учурунда системанын энтропиясынын өзгөрүшү нөлгө барабар болот, б. а. ST=0=0, S=S0=const. Ошентип абсолюттук нөл температурадагы бирдей температуралык жүрүш, бир эле мезгилдерде энтропиялуу да болуп саналат. Термодинамика илимде жана техникада кеңири колдонулат.
Кошумча караңыз
[түзөтүү | булагын түзөтүү]- [[Термодинамикалык тең салмактуулук
]]
Колдонулган адабият
[түзөтүү | булагын түзөтүү]- Физика:Энциклопедиялык окуу куралы. —Бишкек:Мамлекеттик тил жана энциклопедия борбору, 2004. —ISBN 9967-14-010-0
Калып:Термодинамика Физикада катуу ,суюк Жана газдын айырмасы эмнеде